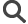Les organoïdes cérébraux et l’intelligence artificielle : de nouvelles perspectives pour le diagnostic de la schizophrénie et des troubles bipolaires
Diagnostiquer la schizophrénie et le trouble bipolaire reste aujourd’hui un défi majeur en psychiatrie. En l’absence de biomarqueurs biologiques fiables, les cliniciens s’appuient essentiellement sur l’observation des symptômes et les entretiens cliniques, avec un risque d’erreurs et de confusions entre pathologies. Une équipe de chercheurs de l’université Johns Hopkins (Baltimore, États-Unis) propose une approche innovante : combiner des organoïdes cérébraux, parfois simplifiés en « mini-cerveaux » – des modèles cellulaires cultivés en laboratoire qui reproduisent certaines caractéristiques du tissu cérébral humain – avec des algorithmes d’intelligence artificielle pour identifier des signatures neuronales propres à chaque trouble. À terme, cette approche pourrait compléter les outils cliniques actuels, en apportant un appui au diagnostic.
La schizophrénie et la bipolarité, des troubles difficiles à diagnostiquer
Aujourd’hui, aucun examen biologique, aucune prise de sang ni aucun test d’imagerie ne permet de poser avec certitude un diagnostic de schizophrénie ou de trouble bipolaire. Ces pathologies reposent sur une évaluation clinique des symptômes, qui peuvent être proches d’autres maladies neurologiques ou psychiatriques. Cette complexité explique les erreurs diagnostiques fréquentes1.
Les organoïdes cérébraux : des modèles cellulaires 3D du cerveau humain
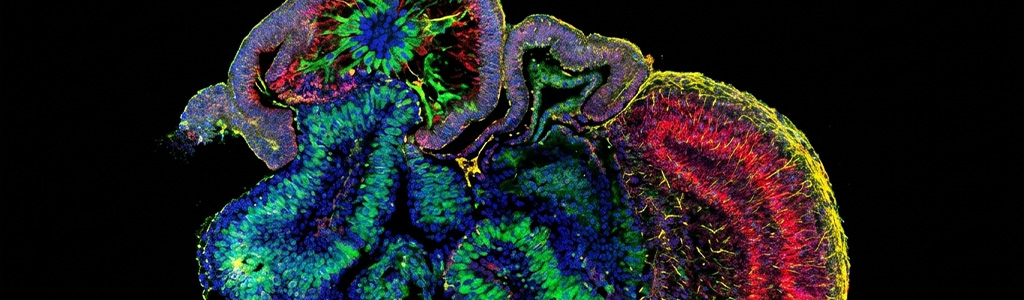
Pour dépasser ces limites, les chercheurs se tournent vers les organoïdes cérébraux. Cultivées en laboratoire à partir de cellules humaines reprogrammées (issues par exemple de la peau ou du sang), ces structures tridimensionnelles reproduisent certaines caractéristiques du cerveau, comme l’organisation de réseaux neuronaux et une activité électrique. Elles ne constituent toutefois ni un organe complet ni un cerveau fonctionnel.
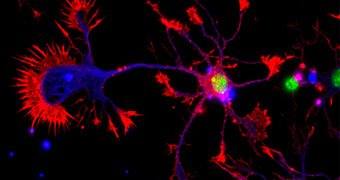
Dans cette étude, les scientifiques ont généré des organoïdes mimant la composition en cellules du cortex préfrontal, une région cérébrale clé impliquée dans la planification, la prise de décision et la régulation des comportements. Ces organoïdes ont été produits à partir de cellules de personnes atteintes de schizophrénie, de trouble bipolaire, mais aussi de personnes sans trouble psychiatrique, servant de groupe contrôle, afin de comparer les résultats1;2.
Quand l’intelligence artificielle « écoute » l’activité neuronale
Les organoïdes ont été enregistrés à l’aide de microélectrodes capables de capter leur activité électrique. Ces signaux ont ensuite été analysés par des algorithmes de machine learning (apprentissage automatique), capables de reconnaître des motifs complexes invisibles à l’œil humain2.
Résultat : les chercheurs ont identifié des signatures électriques distinctes entre les organoïdes sains et ceux issus de patients atteints de schizophrénie ou de trouble bipolaire. Ces différences deviennent encore plus marquées lorsque les réseaux neuronaux sont stimulés par des impulsions électriques, mimant une forte sollicitation du cerveau2.
L’intelligence artificielle parvient ainsi à distinguer des organoïdes de patients schizophrènes de ceux de personnes saines2, en se basant uniquement sur leurs signatures électrophysiologiques. Dans certaines conditions expérimentales, la précision de classification atteint plus de 92 %.
Vers des signatures neuronales des maladies psychiatriques
Ces résultats suggèrent l’existence de véritables « signatures neuronales » propres à chaque trouble. À terme, cette approche pourrait compléter les outils cliniques actuels, en apportant un appui au diagnostic2.
Au-delà du diagnostic, ces organoïdes ouvrent la voie à une nouvelle forme de médecine personnalisée : il devient possib
le de tester différents traitements directement sur les organoïdes issus des cellules d’un patient, afin d’observer leur effet sur l’activité neuronale, sans risque pour la personne. L’objectif n’est plus seulement de traiter les symptômes, mais d’adapter les prescriptions aux réponses biologiques individuelles1,2.
Un enjeu majeur pour les neurosciences et la psychiatrie de demain : la médecine personnalisée
Cette recherche illustre une évolution des neurosciences : le passage d’une psychiatrie fondée uniquement sur l’observation des comportements à une approche intégrant des données biologiques et computationnelles. En combinant organoïdes cérébraux, intelligence artificielle et neurosciences, les chercheurs développent des outils capables de relier le fonctionnement des réseaux neuronaux aux troubles psychiques. À terme, ces approches pourraient transformer la prise en charge des maladies psychiatriques et neurodéveloppementales, en permettant des diagnostics plus fiables, des traitements mieux ciblés et une médecine plus personnalisée.
Sources
-
Published, R. M. C. /. Neural basis of schizophrenia and bipolar disorder found in brain organoids. The Hub https://hub.jhu.edu/2025/09/22/schizophrenia-bipolar-disorder-brain-organoids/ (2025).
-
Cheng, K. et al. Machine learning-enabled detection of electrophysiological signatures in iPSC-derived models of schizophrenia and bipolar disorder. APL Bioeng. 9, 036118 (2025).
Rédigé par Océane Delvarre, scientifique et bénévole au pôle recherche
Photo générée par Gemini et inspirée de la publication Lancaster MA, Renner M, Martin CA, et al. Cerebral organoids model human brain development and microcephaly. Nature. 2013;501(7467):373-379. doi:10.1038/nature12517
Glossaire
Glossaire
- Organoïde : « mini-organe » cultivé en laboratoire à partir de cellules humaines prélevées chez des patients sains ou malades, qui permet de mimer une partie des fonctions de l’organe uniquement.
- Cortex préfrontal : région du cerveau impliquée dans la prise de décision, la planification et la régulation des comportements.
- Machine learning (apprentissage automatique en français): méthode d’intelligence artificielle qui permet à un algorithme d’apprendre automatiquement à identifier des motifs (patterns) et des relations dans de grands ensembles de données. À partir d’un jeu de données d’entraînement, le modèle apprend à reconnaître des caractéristiques pertinentes, puis devient capable de détecter et d’identifier des données d’intérêt dans de nouveaux ensembles de données complexes.
- Membrane Electrode Assembly (MEA) : dispositif composé de microélectrodes organisées en réseau permettant d’enregistrer l’activité électrique des neurones.