Les grandes avancées technologiques en Neurosciences
Sydney Brenner, biologiste sud-africain, prix Nobel de médecine et pionnier de la biologie moléculaire, disait : « Les progrès en sciences dépendent des nouvelles techniques, des nouvelles découvertes et des nouvelles idées, sans doute dans cet ordre ». Depuis toujours, les avancées technologiques ont permis de faire de nouvelles observations, et sont donc un des points clés de l’évolution de nos connaissances en biologie et plus particulièrement en neurosciences. Grâce notamment à l’imagerie de pointe, il est dorénavant possible d’observer le cerveau à plusieurs échelles (macroscopique, microscopique, nanoscopique), mais aussi de visualiser le cerveau en action, ou encore d’enregistrer et de contrôler l’activité neuronale.
-
Enregistrer l’activité des neurones
Une première avancée technologique extrêmement importante pour les neurosciences a été la capacité d’enregistrer l’activité électrique des neurones grâce à des techniques d’électrophysiologie. Parmi elles, l’invention et la mise au point du patch-clamp dans la fin des années 70 a permis pour la première fois de regarder le fonctionnement d’une molécule individuelle, en enregistrant l’activité de canaux ioniques individuels au sein des neurones (protéines membranaires dont l’ouverture déclenchée par des neurotransmetteurs contrôle l’activité neuronale). Cette première technologie d’enregistrement électrophysiologique a ensuite été étendue pour aller enregistrer l’activité d’un neurone à l’intérieur d’une tranche de cerveau. Aujourd’hui, il est même possible d’enregistrer l’activité neuronale sur des animaux vivants, en comportement, ce qui permet de corréler l’activité au fonctionnement plus général du cerveau. Ces techniques sont très largement utilisées pour comprendre le fonctionnement du cerveau mais elles présentent un inconvénient notable : on ne peut enregistrer qu’un seul neurone à la fois. Or, le cerveau est constitué de milliards de neurones et de millions de milliards de synapses (voir encadré ci-contre). Des techniques d’imagerie ont donc été développées dans le but d’avoir une vision d’ensemble du cerveau.
-
La découverte des protéines fluorescentes au service de l’imagerie
Une avancée majeure dans les capacités à imager le cerveau a été la découverte de protéines fluorescences. La première développée il y a environ 40 ans a été la GFP (green fluorescent protein), une protéine de fluorescence verte issue de la méduse et qui a valu à ses inventeurs un Prix Nobel de chimie en 2008. Cette protéine présente des avantages considérables : elle est petite, intrinsèquement fluorescente et elle permet de marquer des protéines spécifiquement pour aller regarder leur localisation et leur organisation dans les neurones. Grâce à ce marqueur fluorescent décliné depuis sous différentes couleurs, les chercheurs ont à leur disposition tout un arc-en-ciel de protéines de couleur pour marquer différentes catégories de cellules.
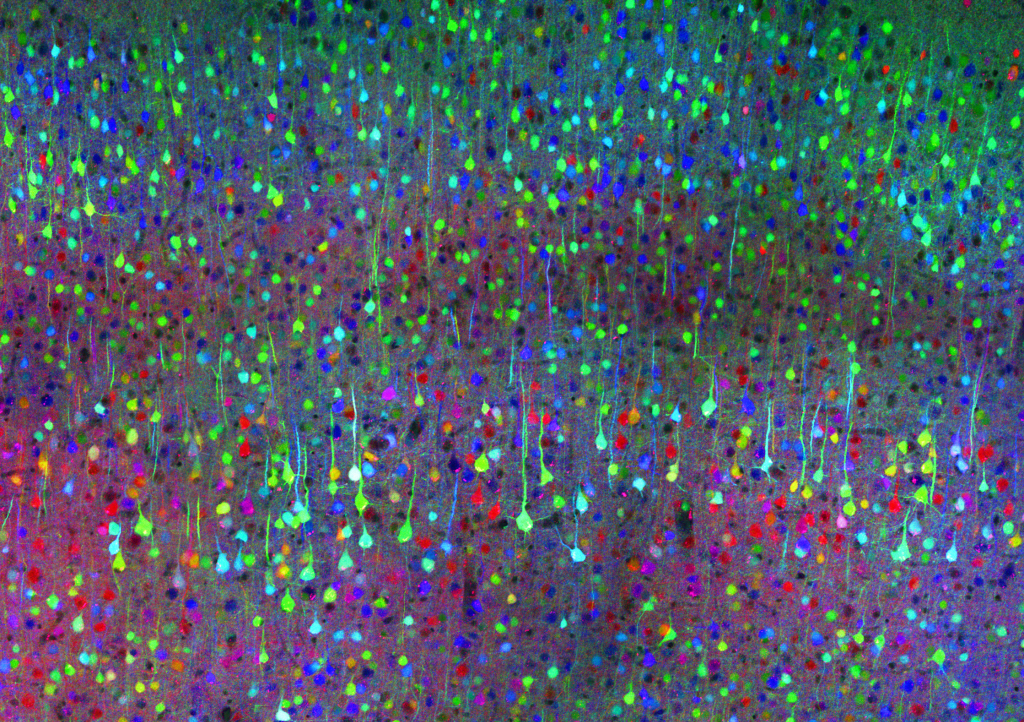
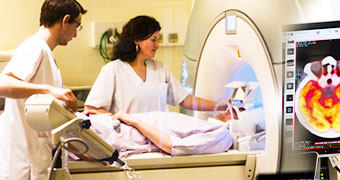
Photographie : « The Brainbow mouse ».
© Inserm/Fouquet, Stéphane
Image d’une coupe de cerveau de la souris arc-en-ciel : les différents types de neurones sont marqués de différentes couleurs. On peut ainsi les distinguer très facilement et étudier leurs fonctionnements ou dysfonctionnements au cours du développement et de la vie de l’animal.
-
Visualiser le cerveau entier, fixé et transparent
Afin d’avoir une vision d’ensemble et regarder comment les neurones sont connectés entre eux, une science se développe : la connectomique. Le problème est que, pour isoler la conduction des influx nerveux, le cerveau est un organe plein de graisses, et donc par définition très peu transparent. Regarder à travers par imagerie est par conséquent un vrai défi. Une avancée importante de ces dix dernières années a été la mise au point des techniques de transparisation et de traçage. Celles-ci permettent de rendre le cerveau transparent grâce à un ensemble de traitements chimiques retirant l’ensemble des lipides. Puis, à partir d’un cerveau rendu fluorescent, elles permettent de regarder les connexions entre différentes régions cérébrales. En utilisant ces techniques avec des microscopes particuliers qu’on appelle des microscopes à feuillet de lumière, les scientifiques sont aujourd’hui capables d’imager un cerveau entier à grande vitesse pour reconstituer les voies de connexions entre différentes aires cérébrales. Cette vision du cerveau est statique, mais il est également important de pouvoir observer le cerveau en action. D’autres techniques ont alors été développées.

Photographie d’un microscope à feuillet de lumière à l’Institut de la Vision.
© Philippe Fraysseix
-
Observer le cerveau en action
Des développements technologiques permettent aujourd’hui d’associer des protéines fluorescentes à des biosenseurs capables de détecter différentes propriétés cellulaires (par exemple détecter les variations de calcium, un indicateur de l’activité neuronale). En exprimant cela dans le cerveau et grâce à des techniques d’imagerie très sophistiquées comme l’imagerie multi-photons, les chercheurs parviennent à mesurer en temps réel l’activité des neurones dans des tranches de cerveaux, et même chez des animaux en comportement. Grâce à des microscopes miniatures très légers (à peine 2g) et indolores appelés miniscopes et attachés sur la tête des modèles animaux, il est désormais possible de filmer et enregistrer l’activité de centaine de neurones en temps réel chez un animal en mouvement. Ces miniscopes donnent ainsi des informations considérables sur le fonctionnement du cerveau. Par exemple, l’enregistrement de l’activité de neurones individuels à l’aide de senseurs calciques chez une souris qui se promène dans un labyrinthe permet de comprendre comment un réseau de neurones va pouvoir traduire une information visuelle en une action motrice de s’orienter à l’intérieur du labyrinthe.

Photographie d’un miniscope.
© Karim Benchenane
-
Voir le cerveau à une échelle nanoscopique
Les techniques précédemment décrites permettent de voir le cerveau de façon dynamique et à l’échelle macroscopique. Mais pour comprendre le fonctionnement du cerveau, les chercheurs ont aussi besoin d’aller regarder à une échelle plus microscopique, au niveau des synapses, pour localiser très précisément les molécules impliquées dans la communication entre les neurones. Ces synapses étant très petites (de l’ordre d’un micromètre, voir encadré ci-contre), elles sont de fait difficilement atteignables par les techniques d’imagerie optique précédemment décrites qui sont limitées par la limite de diffraction (limite qui empêche de distinguer des objets trop proches les uns des autres). Depuis une dizaine d’année, un ensemble de techniques dites de super-résolution ont été inventées et permettent de briser cette limite de diffraction pour voir l’impensable : le fonctionnement intrinsèque des synapses au niveau de molécules individuelles. Ces techniques ont donné lieu à un nouveau Prix Nobel de chimie en 2014. A partir des signaux de molécules individuelles, il est possible de reconstruire la forme de la synapse avec une précision inégalée qui peut atteindre une dizaine de nanomètre (soit un centième de micron, 20 000 fois plus petit que la taille d’un cheveu). Ces techniques de super-résolution peuvent aussi être utilisées sur des neurones vivants. C’est ce qu’on appelle le suivi de particules individuelles, qui permet d’avoir une vision dynamique des molécules à la surface des neurones par exemple.
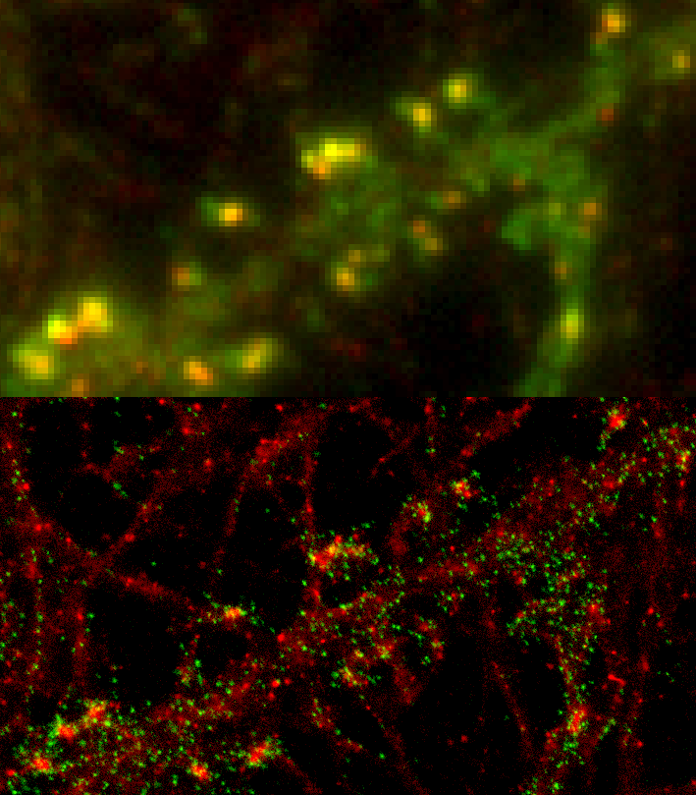
En haut de l’image, on voit une imagerie classique limitée par la diffraction : la synapse, marquée avec 2 protéines (une en vert et une en rouge), apparaît en jaune, on ne distingue pas les détails. En bas, une imagerie en super-résolution qui permet de gagner une précision considérable pour détecter l’organisation nanoscopique de ces synapses et voir toutes les molécules individuelles les constituant : on remarque que les protéines rouges et vertes ne sont pas aux mêmes endroits.
Imagerie classique vs. imagerie en super-résolution.
© Institut Interdisciplinaire des Neurosciences de Bordeaux
-
Contrôler le cerveau en action
En plus de toutes ces techniques d’observation, allant des réseaux de neurones aux synapses individuelles, les scientifiques sont aujourd’hui capables de contrôler le cerveau en modifiant directement son activité grâce aux techniques d’optogénétique, une véritable révolution technologique. Associant l’optique à la génétique, ce système consiste à modifier génétiquement des neurones pour les rendre sensibles à la lumière grâce à l’expression de protéines particulières comme les très utilisées channelrhodopsines. En réponse à des stimulations lumineuses, ces protéines permettent d’activer ou d’inhiber des neurones déterminés, de façon transitoire et sans toucher aux cellules voisines. Associée à un miniscope, l’optogénétique permet par exemple de voir directement les effets d’une activation d’une population de neurone sur un comportement donné chez l’animal. Le développement de cette technique a ouvert la voie vers un nouveau champ d’application très large permettant de mieux comprendre le fonctionnement et les dysfonctionnements du cerveau.
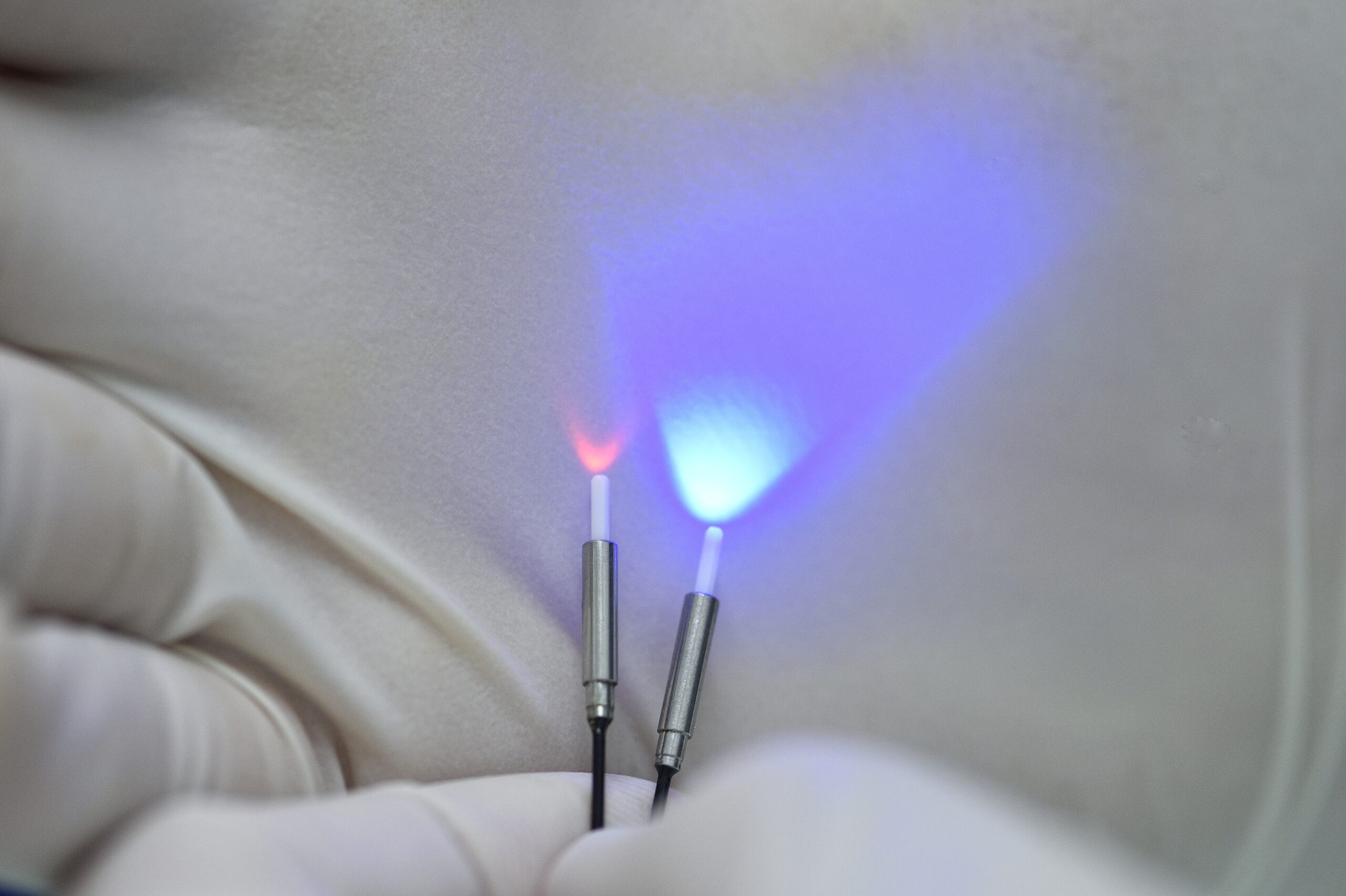
Photographie de fibres optiques délivrant une source lumineuse.
© Inserm/Delapierre, Patrick
En associant les capacités d’imager les neurones à différentes échelles (macroscopique, microscopique, nanoscopique), de façon statique ou dynamique, avec les capacités de modifier l’activité des neurones par l’optogénétique, les chercheurs sont capables d’augmenter considérablement la compréhension du fonctionnement du cerveau. Tout ceci est rendu possible par l’apport de sciences très variées comme la chimie, la physique, les mathématiques ou encore l’informatique, en complément des sciences biologiques. Le développement d’outils technologiques de pointe au service de la recherche sur le cerveau ne cesse de grandir et l’imagerie en neurosciences à encore de beaux jours devant elle.
—
Source/Contenu :
Daniel Choquet – Directeur de l’Institut Interdisciplinaire des Neurosciences de Bordeaux, et du Bordeaux Imaging Center.
Rédaction : Céline Petitgas, chargée des actions scientifiques de la FRC.
Zoom sur notre cerveau
On estime aujourd’hui que le cerveau humain est composé d’environ 86 à 100 milliards de neurones, qui communiquent entre eux au niveau de zones de contacts qu’on appelle des synapses. Chaque neurone serait en moyenne connecté à 1 000 à 10 000 autres neurones, portant le nombre de synapses dans notre cerveau à un million de milliards. Ces synapses sont de la taille d’un micromètre environ, soit un vingtième de cheveu. Ainsi, pour étudier le cerveau, les chercheurs sont obligés de travailler à plusieurs échelles : l’échelle micro/nanoscopique pour regarder comment fonctionne une synapse, l’échelle mésoscopique pour regarder le réseau cérébral formé de ces connexions entre ces milliards de neurones qui communiquent entre eux pour traiter l’information, et l’échelle macroscopique pour comprendre les connexions entre les différentes aires cérébrales.
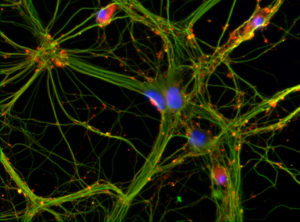
Photograhie d’un neurone
© Inserm/Saoudi, Yasmina

Financement d'équipements de haute technologie
A la suite d’un appel à projet lancé chaque année par la FRC pour le compte de l’association Rotary-Espoir en Tête, le Conseil Scientifique de la FRC expertise et classe par ordre de préférence scientifique les dossiers de projets de recherche reçus par la FRC. Un représentant Rotary-Espoir en tête représente les rotariens français lors du choix des dossiers pendant le Conseil Scientifique.
Spécificité des appels à projets Espoir en Tête : ils ne portent que sur du gros matériel de recherche de haute technologie (microscopes, vidéomicroscope, analyseur métabolique, plateforme de prototypage pour l’étude des neurones…), à l’exclusion de tout salaire ou prestation de services.
> Découvrez l’ensemble des projets financés dans le cadre de l’Appel à Projets Espoir en Tête
Ces projets sont financés grâce à l’opération de collecte organisée par l’Association Rotary-Espoir en Tête chaque année.

Exemple d'un projet financé
Le Dr.Antoine DE CHEVIGNY a reçu en 2019 un financement pour l’achat de deux microscopes miniatures afin d’étudier le cerveau en action.